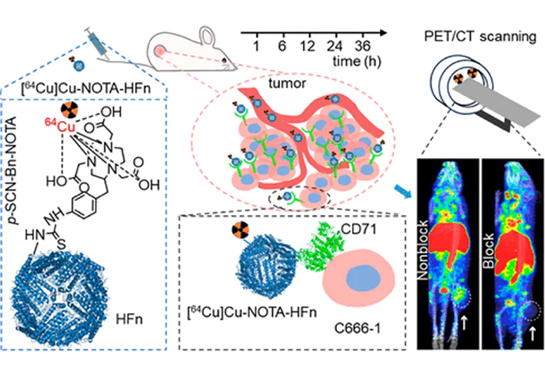
来自中山大学附属第五医院分子影像中心和核医学科的研究团队,最近就[64Cu]Cu-NOTA-HFn合成及用于鼻咽癌转铁蛋白受体 1 表达的 PET 成像评价,在《ACS Omega》上发表了研究报告。
鼻咽癌与转铁蛋白受体1靶点
复发性和转移性鼻咽癌(NPC)是鼻咽癌患者最常见的死亡原因。在组织学上,它可分为三种主要亚型:角化性鳞状细胞癌、非角化性鳞状细胞癌和基底样鳞状细胞癌,非角化亚型进一步分为分化型和未分化型,其中未分化非角化鳞状细胞癌占主导地位,约占病例的 95%,并显示出显着增加的远处转移趋势。然而,肿瘤内的异质性,导致了治疗的不同反应,这种异质性导致大约 15-30% 的患者出现治疗耐药性、复发和转移。这些患者中,中位生存时间仅为 11-28 个月,因此,迫切需要开发针对鼻咽癌的具体诊断方法和有效的治疗干预措施。
正电子发射断层扫描(PET)是一种成熟且有前途的方法,它使用放射性标记的配体以高灵敏度靶向特定分子,从而实现标记物的无创可视化定量分析,用于靶向的肿瘤细胞表面过表达的受体在早期肿瘤发生中起着至关重要的作用,使其成为诊断和治疗的理想靶标。因此,鼻咽癌中过表达细胞膜受体的探索和放射性标记配体的使用为鼻咽癌的早期精确诊断和促进个性化治疗提供了潜力。
转铁蛋白受体 1(也称为分化簇 71、CD71)是一种位于细胞膜上的 II 型跨膜糖蛋白,介导细胞铁摄取。CD71 通常在大多数正常细胞中以低水平表达,但据报道在各种恶性肿瘤中过表达,并在肿瘤增殖、迁移和侵袭中起重要作用。此外,其与临床分期和预后的关联已在研究中得到证实,转铁蛋白受体 1可作为多功能肿瘤标志物。
鼻咽癌分子探针的探索与研究亮点
复发性和转移性鼻咽癌通常是预后效果不佳的主要原因,临床上迫切需要找到更有效的生物分子靶点和开发靶向探针,以便实现早期和特异性肿瘤诊断,并指导个体化治疗。
CD71 是一种负责介导细胞铁摄取的 II 型跨膜糖蛋白,通常在肿瘤中过表达;HFn 是一种天然且生物相容的铁储存蛋白,已被证明可通过 CD71 与人体细胞结合,研究者证实了 NPC细胞中CD71 和 HFn-FITC 摄取的高表达,基于这些发现,中山大学附属第五医院分子影像中心金红军教授和核医学科王颖主任带领的研究团队开发了一种新的放射性示踪剂[64Cu]Cu-NOTA-HFn,使用放射性核素Cu-64标记的HFn靶向CD71,用于NPC的无创诊断。
亮点1:分子结构特点与优势
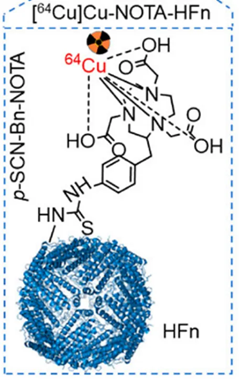
HFn成为CD71的最佳配体:基于各种靶向CD71的结合剂中,HFn具有良好的生物相容性和对CD71的固有靶向特异性;其24个亚基可以自组装,可实现药物的可控封装和释放;其与CD71结合时表现出阈值依赖性内化,增强了其体内肿瘤选择性和生物安全性;此外,HFn与CD71的结合位点,使其对转铁蛋白Tf与CD71结合介导的细胞铁获取的生理过程的干扰最小。
双功能螯合剂(如NOTA和DOTA):与以前的HFn内部装载方法不同,通过游离赖氨酸残基用这些双功能螯合剂修饰HFn的外表面,可以有效地将Cu-64标记到HFn上。这种螯合剂蛋白标记方法不占用HFn的内腔,允许装载其他药物,因此为联合治疗提供了思路,未来有望实现HFn介导的癌症的治疗。
有利的靶点与非靶点比率:选择半衰期与HFn相似的放射性核素至关重要。HFn的血液清除半衰期约为4小时,而非常适合PET成像的Cu-64,半衰期为12.7小时,可以充分消除背景组织中的非特异性放射性。
[64Cu]Cu-NOTA-HFn分子体外稳定性:由于HFn的固有稳定的纳米笼结构而具有良好的稳定性。体外溶解度和稳定性实验表明,[64Cu]Cu-NOTA-HFn具有高水溶性(log P=−2.42±0.52,n=6)和在磷酸盐缓冲盐水(PBS)中长达48小时的良好稳定性。
亮点2:标记方法学
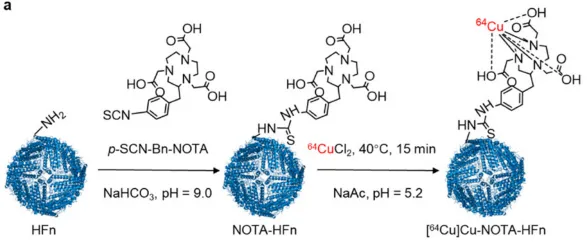
[64Cu]Cu-NOTA-HFn的整个放射性标记过程在15分钟内完成,产率高(>98.5%),摩尔活性高(72.96±21.33 GBq/μmol)。
[64Cu]Cu-NOTA-HFn具有较高的放射化学标记率和体外稳定性,为进一步转化或临床应用提供了基础。
通过类似的标记方法,多种有前景的成像同位素,如Zr-89,以及治疗同位素,如Lu-177、Y-90和Cu-67,可以标记HFn纳米笼,用于不同的应用。
亮点3:NPC肿瘤靶向特异性
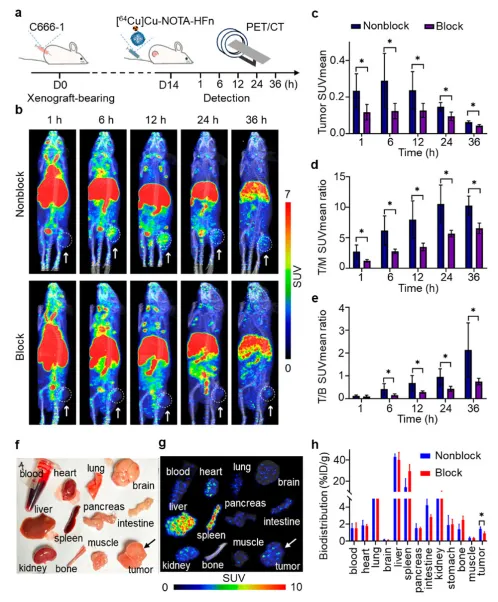
在体外对C666-1细胞表现出高的结合亲和力和特异性:细胞饱和结合测定表明[64Cu]Cu-NOTA-HFn对过表达CD71的C666-1细胞具有纳摩尔亲和力(Kd=10.9±6.1 nM)。
在NPC荷瘤小鼠体内的肿瘤靶向特异性:为了在体内测试靶点结合,在C666-1 NPC荷瘤小鼠注射[64Cu]Cu-NOTA-HFn后1、6、12、24和36小时进行长时间PET成像。C666-1肿瘤可通过[64Cu]Cu-NOTA-HFn显示,并通过非放射性标记的HFn阻断。PET成像定量分析表明,C666-1肿瘤对[64Cu]Cu-NOTA-HFn的摄取在注射后6 h达到峰值,最佳放射性肿瘤与肌肉的比值为10.53±3.11(n=3)。注射后6 h时的离体生物分布测定显示,非阻断组的肿瘤摄取量为1.43±0.23%ID/g,阻断组为0.92±0.2%ID/g(n=3,p<0.05)。
[64Cu]Cu-NOTA-HFn对CD71阳性的NPC肿瘤具有非常高的靶点结合,为进一步的临床转化提供了基础。
不足与未来方向
在[64Cu]Cu-NOTA-HFn用于鼻咽癌的临床前评价研究中,研究者证明,通过 PET 成像无创检测 CD71 表达 [64Cu]Cu-NOTA-HFn可能是诊断鼻咽癌的一种方式。
然而,[64Cu]Cu-NOTA-HFn相对较高的肝脏和脾脏积累水平仍然是当前研究和进一步治疗实验的主要限制。研究团队推断其可能的原因:首先,肝脏对Cu-64摄取的增加很可能是由游离的Cu-64造成的,大环铜螯合物限制了肝脏中超氧化物歧化酶的体内稳定性,为了防止脱标,必须开发新的方法来阻止铜离子的还原或改善亚铜离子的配位;其次,肝脏和脾脏是铁蛋白纳米粒子代谢的主要器官,因此表现出强烈的HFn积累。
为了有效减少肝脏对纳米材料的吸收,拟计划开展:(1)增加流速以降低纳米材料螯合的可能性;(2)改变关键细胞的表型以降低它们对纳米材料的亲和力,以确定是否可以减少肝脏和脾脏中HFn的摄取。
同时,研究者将进一步优化探针,以提高靶点与非靶点的比率,用于未来在CD71过表达肿瘤患者中的临床应用。