概述:
帕金森病(PD)是一种神经退行性疾病,发病机制主要有以下几个特征:如黑质神经元丧失、纹状体多巴胺功能降低以及富含α突触核蛋白的路易小体的形成等,而α-突触核蛋白的SNCA突变又是家族性PD的已知原因,当SNCA基因中的G51D突变出现时,就会迅速加重PD病情的恶化。最近,科学家通过CRISPR/Cas9技术成功的将G51D突变导入了内源性大鼠SNCA基因中,通过对这一基因突变大鼠的观察,他们发现这一模型呈现出与PD高度相关的早期疾病表型。在研究中,科学家对野生型(WT)、SNCAG51D/+和SNCAG51D/G51D大鼠进行了衰老过程(5、11和16个月)的观察,并使用放射性示踪剂18F-DOPA对模型大鼠进行动态 PET成像和建模,通过PET数据的分析,他们成功确定了与PD早期症状高度相关的生化特征变化。
这一突破性的大鼠模型为帕金森病的早期检测提供了新的方法,也为我们更好地了解这种疾病的起源和发展提供了有力证据。
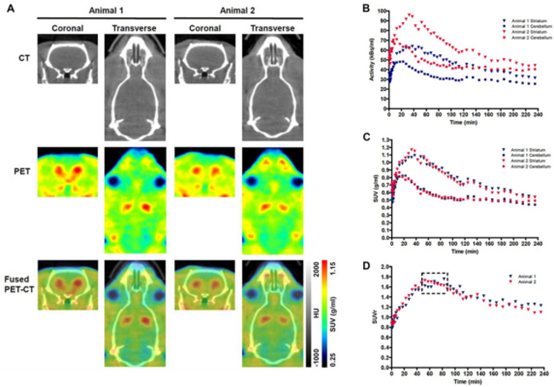
上图,野生型(WT)大鼠PET-CT图像、标准化摄取值(SUV)和时间活动曲线(tac)。
(A) WT大鼠的冠状面和横切面PET-CT图像,图中显示两只WT大鼠纹状体相对于小脑对18F-DOPA的特异性摄取的比活性(B)、SUV TAC数据(C)和SUV比率(SUVr)数据(D)。虚线框表示伪平衡阶段(50-85 min)。
18F-DOPA PET成像显示多巴胺转换缺陷
为了研究大脑在不同年龄和基因型下的差异,研究人员使用了18F-DOPA PET成像技术,分别对对不同年龄(5、11、16月龄)的WT大鼠、SNCAG51D/+大鼠和SNCAG51D/G51D大鼠进行了扫描,每个年龄组每个基因型4只大鼠。结果表明16个月SNCAG51D/G51D大鼠的平均多巴胺转换与年龄匹配的WT大鼠相比有所增加。通过对大鼠模型进行研究发现,早期帕金森氏症大鼠的大脑中多巴胺转换缺陷存在不对称性,这也意味着在帕金森氏症的早期阶段,大脑某些区域的多巴胺水平会下降,而另一些区域则相对健康。
结论:
据体内PET/CT成像结果显示,SNCAG51D/G51D大鼠在16月龄时,其纹状体多巴胺转换明显增加,但Ki-多巴胺合成和储存并未明显减少。这一发现模拟了帕金森病的早期阶段,这一情况有可能在人类患者中观察到的多巴胺系统的代偿性变化有关。总之,SNCAG51D大鼠作为早期帕金森病病理生理模型,对于研究帕金森病中其他遗传或环境触发因素提供了一个方便的平台。这项研究揭示了帕金森病早期的神经变化,同时也为帕金森病研究带来了新的应用前景。
研究团队:
英国爱丁堡大学生物科学学院
爱丁堡大学生物科学学院在教学、研究和创新方面始终处于领先地位。《泰晤士报》一直将该学院列为全球生物科学领域排名前25位的大学之一。,同时,爱丁堡大学生物科学学院也是英国质量最高、影响力最大的生物系之一。在2014年英国国家研究评估中,超过一半的研究活动在质量和范围上被评为“世界领先”,在英国大学教学领域排名第三和第二。