Iomab-B (131I-apamistamab)的个性化给药已被证明能够成功地使患有活动性疾病的复发和/或难治性急性髓细胞白血病(AML)患者成功地接受可能挽救生命的骨髓移植。随机、多中心III期SIERRA试验显示,骨髓移植前使用Iomab-B的一年生存率是常规治疗的两倍,超过60%的患者在6个月时实现了持久的完全缓解,并维持两年或更长时间的生存期。这项研究在核医学和分子成像学会2023年年会上发表,并被选为会议的年度摘要。
每年,SNMMI都会选择一篇最能体现核医学和分子成像领域最具前沿进展的摘要。今年,SNMMI Henry n . Wagner Jr .的年度摘要是由评审人员和学会领导层投票,从提交给会议的1500多篇摘要中选出。
AML是成人最致命的白血病之一。美国癌症协会估计,2023年将有20,380人被诊断患有AML,超过11,300人将死于该疾病。AML患者中的大部分人都属于复发或难治性疾病患者。
纪念斯隆-凯特琳癌症中心放射科分子影像和治疗服务部主治医师、纽约州纽约市Weill Cornell医学院教授Neeta Pandit-Taskar博士指出:“患有活动性、复发/难治性AML的老年患者预后非常差,目前的治疗选择非常有限。在常规的临床实践中,这些患者不被考虑进行潜在的治疗性骨髓移植。”
在这项研究中,来自美国和加拿大24个中心的研究人员调查了Iomab-B向白血病细胞提供高剂量靶向辐射以使患者能够接受骨髓移植的安全性和有效性。试验招募了55岁或以上患有活动性、复发性或难治性AML的患者参与受试。76名患者被随机分配接受个体化剂量的Iomab-B,然后进行骨髓移植,77名患者接受医生选择的常规治疗(高剂量化疗)。接受常规治疗并获得完全缓解的患者接受了骨髓移植;那些在常规治疗后没有反应或疾病进展的患者有资格转入研究Iomab-B组。研究评估了Iomab-B的安全性,并对两组患者进行了随访,以确定持久完全缓解的比率(从骨髓移植后最初的完全缓解开始维持6个月的完全缓解)
所有接受Iomab-B治疗剂量的患者都进行了骨髓移植,而只有常规治疗的患者中只有14名患者接受了骨髓移植。44名常规护理患者转入了Iomab-B组后,其中40人在接受了Iomab-B给药后,能够进行骨髓移植。
使用Iomab-B进行治疗能够安全地向白血病细胞提供高剂量的靶向辐射,从而实现骨髓移植成功。六个月持久完全缓解的主要终点明显支持IOM ab-B(22 %)而不是常规治疗(0%)。
Pandit-Taskar博士说: “这项关键的研究表明,单次个性化剂量的Iomab-B使所有接受治疗剂量的患者都能获得潜在的治愈性骨髓移植,相比之下,接受常规治疗的患者中只有17%获得骨髓移植。 Iomab-B还证明了符合主要终点的患者的长期生存受益,并且Iomab-B主导的方案的安全性非常好。“此外,核医学的可见性和交叉功能性得到了明确展示,加强了核医学、护理和移植团队之间的合作。这将进一步推动核医学在放射免疫靶向治疗规划和管理中的应用。
SNMMI科学项目委员会主席Heather Jacene医学博士表示:“这项试验的结果表明,核医学在帮助改变白血病患者的预后方面做出了重大贡献。复发或难治性疾病患者是AML中最大的一部分,在这10000名左右的预估患者中,有很大一部分可能受益于本试验的结果。”
Iomab-B的生物制剂许可申请将于2023年底前提交给美国食品药品监督管理局(FDA)。随着FDA的潜在批准,Iomab-B有希望在2024年下半年上市。此外,预计2023年,美国的研究机构将为复发或难治性急性髓细胞白血病患者提供扩大治疗计划。
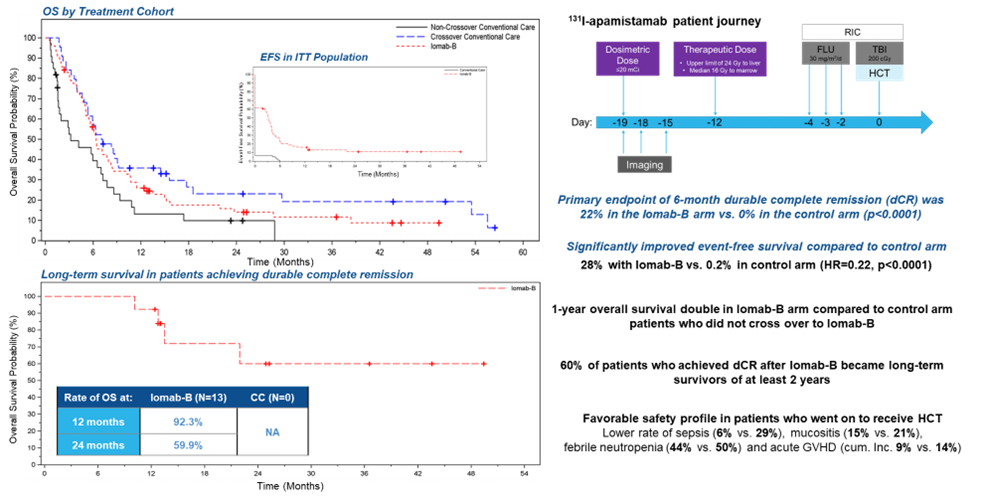
接受Iomab-B治疗的患者在接受骨髓移植后的总生存期(OS)、无事件生存期(EFS)和安全性方面的改善,患者的长期生存率达到了持久完全缓解的主要终点。
Abstract 685. “Individualized dosing for high-dose targeted radiation of hematopoietic cells with Iomab-B (I131-apamistamab) prior to HCT in relapsed/refractory acute myeloid leukemia (R/R AML): Safety and efficacy results from the pivotal phase 3 SIERRA trial.” Neeta Pandit-Taskar,Memorial Sloan Kettering Cancer Center, New York, New York; Mona Natwa, The Ohio State University Wexner Medical Center, Columbus, Ohio; Ming-Kai Chen, Yale School of Medicine, New Haven, Connecticut; Robert Wagner, Loyola University Medical School, Maywood, Illinois; Wendell Yap, University of Kansas Medical Center, Kansas City, Kansas; Landis Griffeth, Baylor University Medical Center, Dallas, Texas; Gregory Wiseman, Mayo Clinic, Rochester, Minnesota; Joyce Mhlanga and Richard Wahl, Mallinckrodt Institute of Radiology, Saint Louis, Missouri; Norbert Avril, University Hospitals Cleveland Medical Center; Cleveland, Ohio; Dominick Lamonica, Roswell Park Cancer Comprehensive Cancer Center, Buffalo, New York; Hubert Vesselle, University of Washington Medical Center, Seattle, Washington; Beth Chasen, MD Anderson Cancer Center, Bellaire, Texas; Craig Johnson, University of Nebraska Medical Center, Omaha, Nebraska; Neil Hansen, University of Nebraska Medical Center, Bennington, Nebraska; Eugene Leung, The Ottawa Hospital, Ottawa, Ontario, Canada; Joseph Osborne, New York Presbyterian Hospital (Cornell Campus), New York, New York; Jennifer Peterson, Mayo Clinic Jacksonville, Jacksonville, Florida; Yusuf Menda, University of Iowa, Iowa City, Iowa; Dinko Franceschi, Stony Brook University Hospital, Stony Brook, New York; Avinash Desai, Patrik Brodin, Elaina Haeuber, and Akash Nahar, Actinium Pharmaceuticals, New York, New York; and Susan Passalaqua, Banner MD Anderson Cancer Center, Gilbert, Arizona.