概述:
抗体生物工程的发展促进了定制靶向抗体的开发和应用,而基于这些定制化的靶向抗体药物正电子发射断层扫描(PET)可以帮助我们更好地了解它们在体内的生物学功能。在这项研究中,我们报告了一项体内预靶向免疫PET成像的验证研究,在此,我们比较了逆电子需求Diels-Alder (IEDDA)在体内点击反应中,使用一种新的89Zr标记的四嗪作为生物正交配体的预靶向和靶向方法,我们采用在头颈部鳞状细胞癌(HNSCC)的免疫pet成像中具有潜力的CD44V6嵌合单克隆U36作为靶向抗体,使用长半衰期锆-89 (t1/2 = 78.41 h)作为首选放射性核素,以便能够对预靶向和靶向方法进行正交实验,我们首先在HNSCC异种移植物(VU-SCC-OE)模型小鼠注射反式环烯(TCO)功能化U36抗体24小时或48小时后,注射[89Zr]Zr-DFO-PEG5-Tz ([89Zr]Zr-3),待未反应的[89Zr]Zr-DFO-PEG5-Tz ([89Zr]Zr-3)从体内清除后,进行预靶向PET成像,成像结果发现预靶向方法的绝对肿瘤摄取比靶向方法低(72 h p.i U36时1.5±0.2 vs 17.1±3.0% ID/g),但肿瘤与非靶组织的比例相当,吸收剂量显著降低,这表明,89zr 标记的抗CD44v6单克隆抗体U36可成功用于HNSCC异种移植肿瘤的靶向和预靶向免疫PET成像,这些结果不仅支持了预靶向方法在免疫PET成像中的应用,而且还可用于监测在体内实现与抗体药代动力学相关的最佳IEDDA反应效率的研究。
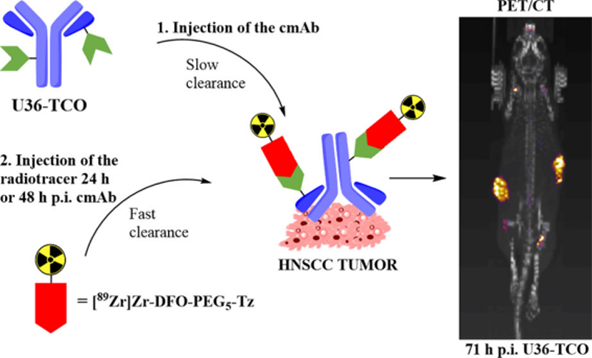
如图所示为U36抗体给药后71小时各组异种移植VU-SCC-OE的冠状位PET/CT图像。尽管预先靶向肿瘤中的活性浓度较低,但由于背景更低,因此肿瘤在PET/CT (PET/CT)上清晰可见(右图)。
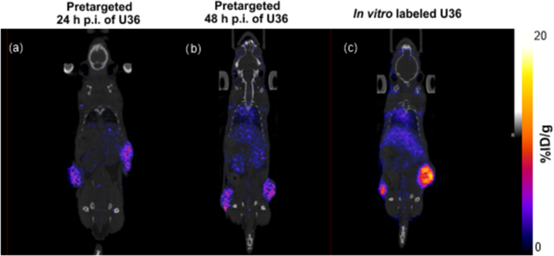
上图,注射U36抗体后71 h,各组的冠状位PET/CT图像;[89Zr]Zr-3以[89Zr]Zr-3与u36的比例为1:1注射(a) 24 h或(b) 48 h p.i. TCO-U36。第三组(c)在t = 0时注射体外标记的[89Zr] Zr-3-TCO-U36。
结论:
采用靶向和预靶向两种方法,抗CD44v6单克隆抗体U36均可成功用于头颈部鳞状细胞癌异种移植肿瘤的89zr -免疫PET成像。我们的研究结果表明,四氮[89Zr]Zr-3预靶向TCO-U36是一种很有前途的概念,可以用于锆-89抗体的体内预靶向PET成像,并且值得进一步研究使用寿命较短的PET放射性核素(如68Ga)进行放射性标记。同时本文提出了一种利用IEDDA和[89Zr]Zr-3对89Zr标记的放射免疫偶联物进行体外放射性标记的新方法。
研究机构:
阿姆斯特丹UMC,阿姆斯特丹自由大学,是享誉世界的一流研究型大学,世界百强名校,其中放射与核医学部是荷兰放射学、核医学和医学成像方面的顶尖院系,学院利用最先进的成像技术进行的研究和创新有助于改善医疗保健,尤其是成像诊断、图像引导和放射性核素治疗。该部门开发了欧洲首屈一指的医学成像研究项目之一,世界范围内具有很高排名。这一成就的来源于多样化的研究项目,包括许多关键的临床和基础研究主题,每年发表约300篇科学论文。该院系为大约100名博士生提供了培训和研究机会。我们的研究人员专注于理解和可视化疾病的分子机制,开发精确诊断工具,包括用于疾病预测、疾病评估和治疗监测的定量成像生物标志物,以及放射性核素疗法的创新