Azalea A. Khan, Francis Man, Farid N. Faruqu, Jana Kim, Fahad Al-Salemee, Amaia Carrascal-Miniño, Alessia Volpe, Revadee Liam-Or, Paul Simpson, Gilbert O. Fruhwirth, Khuloud T. Al-Jamal, and Rafael T. M. de Rosales* February 28, 2022
概述:
外泌体是一种小的细胞外囊泡(sEV),是由细胞衍生的双层磷脂包裹的纳米小泡,为大多数内分泌细胞分泌,sEV尺寸较小(30–150 nm),其特征是存在特定的膜标记蛋白,如CD63、CD9、Alix和TSG101.2,sEV的主要作用是细胞之间胞质分子(即核酸、脂质、蛋白质等)的运输和交换,因此在细胞-细胞通信和疾病进展中充当信使,例如,肿瘤细胞sEV可促进肿瘤细胞增殖和转移,并诱导抗肿瘤药物耐药性。有趣的是,天然和载药sEV(来源于干细胞、免疫细胞或癌症细胞)在癌症、阿尔茨海默病、型糖尿病和II型糖尿病中显示出治疗潜力,此外,它们具有跨越血脑屏障(BBB)和选择性靶向组织的能力,因此,人们对使用sEV作为纳米治疗药物越来越感兴趣。因此,开发跟踪sEV体内行为的成像手段就非常重要,这样将提高我们对其生物学的理解,并支持其作为药物递送工具的发展。
对于sEV在体内的示踪手段必须满足在一段时间内对动物全身进行跟踪,因此,研究团队想到了利用正电子发射断层成像(PET)搭配长半衰期核素的示踪手段,在本报告中,研究团队探索了[89Zr]Zr(oxinate)4(一种细胞和脂质体放射性示踪剂)用于几种类型的sEV的直接和腔内放射性标记的用途,实现了高放射性标记产率。如使用几种表征(冷冻电镜、纳米颗粒跟踪分析、斑点印迹和流式细胞术)和体外技术所证明的那样,对sEV标记的放射合成和放射标记方案进行了优化,避免了sEV损伤。通过建模胰腺癌sEVs(PANC1)小鼠进行PET成像,研究团队表明在小鼠体内使用89Zr标记的sEVs可进行至少24小时的PET示踪,此外,研究团队还报告了sEVs与热损伤sEVs的生物分布差异,并发现后者在脾脏摄取显著减少。因此,我们得出结论,使用这种方法进行89Zr标记的sEV可以可靠地用于体内PET示踪,从而可以有效地探索其作为药物递送系统的潜力。
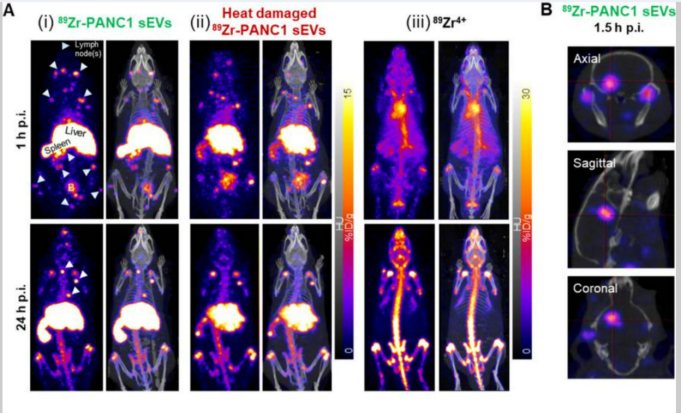
89Zr-PANC1 sEV的PET成像。(A) C57BL/6j小鼠静脉注射89Zr-PANC1 sEV后1小时和24小时成像(i),热损伤89Zr-PANC1 sEV(ii)和NaOH中和的89Zr4+(iii)的PET-CT成像;白色箭头代表性LNs,B为膀胱;(B) 注射89Zr-PANC1 sEV小鼠大脑内摄取的PET-CT图像(轴向、矢状和冠状切片)。
研究团队:
伦敦纳米技术中心是一家总部位于英国的多学科研究机构,其通过应用纳米科学和纳米技术来解决信息处理,医疗保健,能源和环境方面的全球问题,始终处于科学和技术的最前沿,2018年伦敦国王学院加入并展开合作。
该中心在化学、物理、材料、医学、电气和电子工程、机械工程、化学工程、生物化学和生物医学工程以及地球科学方面与企业、投资和工业合作伙伴有广阔的合作前景,并始终保持最前沿的纳米技术。