摘要:
调节性T细胞(Tregs)是一种有前景的候选细胞疗法,用于治疗自身免疫性疾病,并有助于移植实体器官的寿命。尽管使用人Treg治疗的临床试验数量不断增加,但有关其体内的作用机制、分布和功能等重要问题仍然没有得到解答。研究发现,病灶组织中Treg的积累对Treg治疗效果至关重要,但现有的血液生物标志物不太可能准确反映其在组织中的分布状态,然而想要解决上述问题,分子影像方法无疑是最具前景的研究手段,通过长半衰期的放射性核素89Zr直接标记Treg,采用正电子发射断层扫描(PET)就可以实现对其进行一周以上的体内追踪,用于评估89Zr多克隆Treg的体内的分布与摄取。研究团队使用[89Zr]Zr(oxinate)4作为细胞标记物,成功实现了人体Treg细胞在0.1-11.1 Bq 89Zr/Treg细胞的放射标记效率,这一剂量将满足超过一周的PET体内细胞跟踪。研究团队还对89Zr Tregs进行了表征,评估了它们的表型,发现这些放射性标记的Treg细胞对89Zr表现出不耐受,因此89Zr多克隆Treg不能以89Zr的半衰期来评估标记物在体内的存活时长和扩散状况。此外,研究团队还通过PET成像发现在体内过继移植8放射性标记物后,89Zr-Treg出现死亡迹象,因此,由于89Zr Tregs的存活率和扩散问题,数周内体内对89Zr/Treg细胞的跟踪并未达到预期结果。最终我们得出结论,间接Treg标记可能是更符合中长期细胞追踪的方案。
移植器官内Treg的比例和移植物存活率存在一定的相关性,研究团队主导的临床试验数据表明Treg疗法的安全,耐受性良好且有疗效,并且通过全身PET成像进行细胞追踪可以观察和解决Treg在体内分布和代谢等重要问题。利用89Zr对多克隆Treg的放射性标记,通过PET/CT可对其进行一周以上的体内追踪。
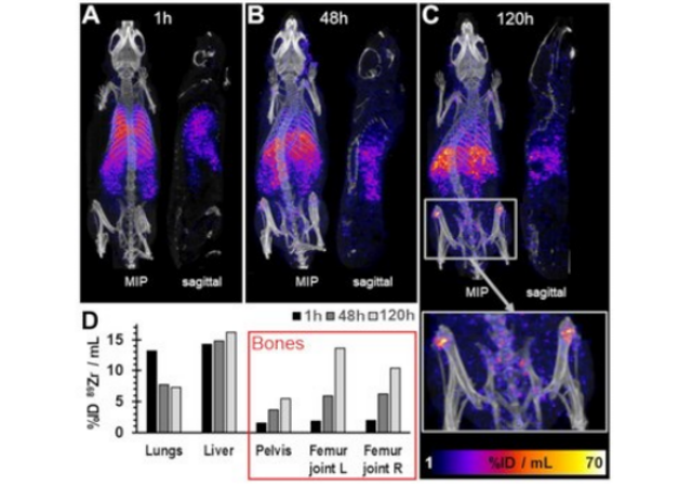
小鼠麻醉后进行89Zr Tregs和HLA-A2阴性CD25-PBMC共同给药到尾静脉,给药45分钟后进行CT图像采集,60分钟后进行PET图像采集。后续分别于给药48小时,120小时进行成像。
体内PET/CT成像结果表明,89Zr-Tregs最初符合静脉注射细胞的预期表现,即它们在给药1小时后积聚在肺部,在之后的一天内它们中的大部分在肺部清除,并在体内其他地方重新分布,有趣的是,Treg在骨骼中的积聚出乎意料之外。此外,随着时间的推移,它们在全身的骨骼中显著增加,据推测,这应该些来自骨骼的89Zr信号应该与游离的89Zr快速矿化有关,这表明89Zr从89Zr- treg流出(从而失去跟踪treg的能力)或89Zr- treg在给药5天后伴随游 treg的死亡而出现游离的89Zr。
团队:纪念斯隆-凯特琳癌症中心是世界上历史悠久、规模弘大的私立癌症中心。130余年来,该中心一直致力于卓越的患者护理,创新的研究和一流的医学教育项目,现已成为美国国家癌症研究所(National Cancer Institute)指定的45所综合癌症中心之一,迎来了先进科学、临床研究和治疗的蓬勃发展。